日前,广东医科大学医学技术学院皮江博士团队,联合中山大学曾谷城教授团队和美国伊利诺伊大学ling shen教授团队在journal of nanobiotechnology(if=10.435,中科院大类学科分类为1区)发表了题为“nanocages engineered from bacillus calmette-guerin facilitate protective vγ2vδ2 t cell immunity against mycobacterium tuberculosis infection”的研究论文,报道了利用生物纳米技术改造卡介苗(bacille calmette- guerin,bcg)为纳米级颗粒,并将其作为潜在结核疫苗的新技术。
结核分枝杆菌感染引起的结核病目前是全球仅次于新冠肺炎的传染病头号杀手(全球约四分之一的人口感染了结核分枝杆菌)。目前,bcg仍然是全球唯一被用于临床的结核疫苗,但bcg经皮内接种仅能有效预防儿童结核病,对成人结核病保护效果却较差。美国哈佛大学的zheng w. chen教授团队(shen et al., science. 2002)和美国nih的robert a. seder团队(darrah et al., nature. 2020)均证实:静脉注射bcg进行免疫接种可有效保护猕猴的结核分枝杆菌感染,改变接种途径显示了bcg更有效的抗结核疫苗应用前景。然而,人体经静脉注射接种bcg具有极大的细菌感染风险,也极易引起不可控的过激免疫反应,如何将bcg开发成可用于静脉注射的潜在疫苗仍是一个难题。
该研究中,作者将bcg细胞壁清除后,通过生物纳米技术将1-5微米大小的bcg原生质体改造成约200纳米的bcg原生质体纳米颗粒(命名为bcg-nanocage),bcg-nanocage保留了bcg的高巨噬细胞靶向作用和激活巨噬细胞抗结核免疫作用的功能,而细胞毒性却较bcg显著降低。bcg-nanocage在体外和猕猴体内均可显著诱导出vγ2vδ2 t细胞免疫反应,接种bcg-nanocage猕猴受到结核分枝杆菌攻击时,vγ2vδ2 t细胞能快速聚集到肺部以抵抗感染,从而有效清除猕猴肺部结核分枝杆菌、并保护其肺部病理损伤。这项研究预示生物纳米技术在疫苗构建和改造中广阔的应用前景,并为更有效的结核疫苗开发提供了新的方向。
广东医科大学医学技术学院的皮江博士为本文第一作者兼共同通讯作者。该研究得到国家自然科学基金(项目编号:81801649、82072250、81870016、1570009、81273237)、广东省自然科学基金(2015a030313513、2020a1515010283)、广东省教育厅普通高校特色创新项目(2021ktscx038)、松山湖材料实验室开放课题(2021slabfn10)、广东医科大学博士科研基金(4sg21236g)的大力支持。(文/张俊爱 编/王丽君 审/冯锦山 )
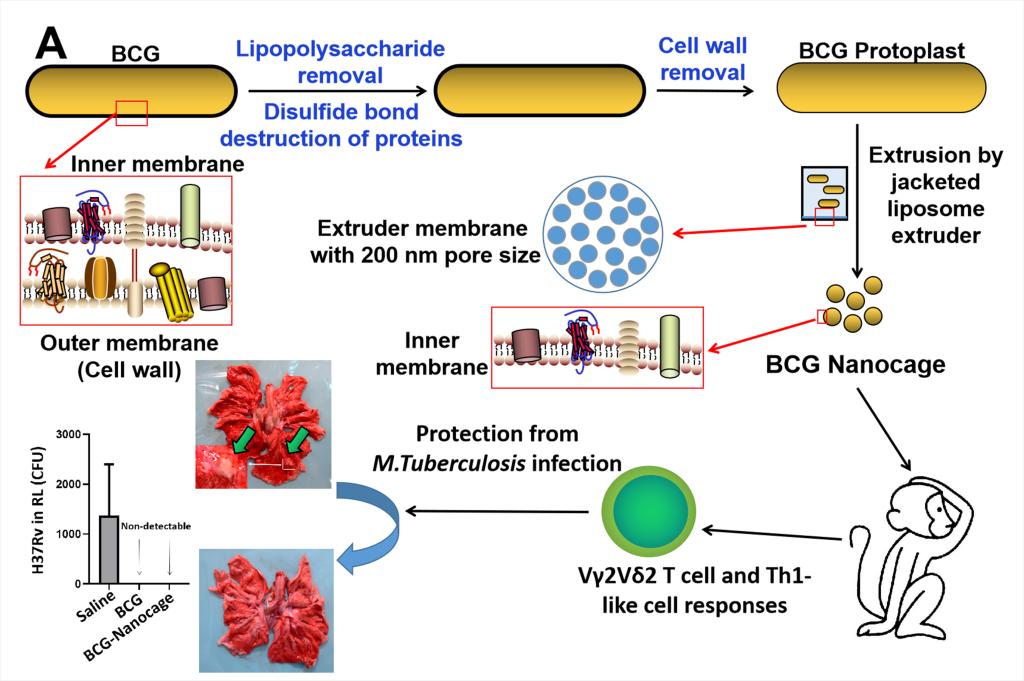
bcg改造及抗结核疫苗应用示意图
原文详见:https://jnanobiotechnology.biomedcentral.com/articles/10.1186/s12951-021-01234-3





